王俊科,叶铁虎,许幸(执笔人),吴新民(负责人),徐建国
阅读 2699
一、引言
吸入麻醉药物的发明标志着现代麻醉学的诞生,它极大推动了现代医学的进步和人类社会文明程度的提高。吸入麻醉药除了麻醉作用,对人体是否有危害或其程度如何一直是令人关心的问题,为此吸入麻醉药经历了不断的更新。另外,吸入麻醉药历来无例外地都是人工合成的化学品,对大气环境的影响也日益引起公众的关注。已知当今的卤族吸入麻醉药物和笑气均属于温室气体,破坏臭氧层。笑气产生温室气体效应的分子强度是CO2的230倍,贡献了全球升温效应的0.1%,而更糟糕的是其在自然界分解的时间长达120年。
然而,吸入麻醉气体在麻醉过程中,不可避免地最终排入大气。不可避免性体现在这些气体在人体内的代谢量很少,病人麻醉后苏醒最终依赖于通过呼吸以原形全部呼出,排向大气。另外,在吸入麻醉实施过程中,或多或少总有部分麻醉气体泄漏,在目前的技术条件下,并不能杜绝此泄漏,这也成为不可避免。麻醉气体泄漏对健康的危害性如何,尤其受到麻醉科医师、手术护士、麻醉恢复室和ICU医护人员的关注。迄今国内这方面缺少系统、严谨的研究,仅在先进国家的有较完整的研究,故中华医学会麻醉学分会组织专家制定了《关于处理麻醉气体泄漏的指导意见》。指导意见将参照目前现有的研究成果和公认的做法,并随相关研究的深入而不断改进。
由于有些问题迄今仍有争论,不能做出确定性的结论,指导意见对这类问题不拟采取回避态度,而是列出相关研究结果和专家意见,以求做到客观、全面,并列出相关参考文献,也为今后的研究进步奠定基础。
指导意见的目的是澄清既往的模糊认识、制定国内需要遵循的标准和应该接受的做法,最大程度地保护暴露人群的健康和我们的生活环境。
用吸入麻醉药对细菌和哺乳动物细胞进行了致突变性的检验。这些研究的共同结论是:笑气、氟烷、安氟烷、异氟烷、七氟烷和地氟烷都没有潜在的致突变性。且绝大多数对DNA损害测试的结果都呈阴性。只有三氯乙烯和三氟乙基乙烯醚是致突变原,但这些药物目前已经废弃。
在啮齿类动物中进行了致癌性研究。观察了长期暴露于微量麻醉废气对机体的影响,在18个月或更长时间内每周多次给予动物麻醉药物。而且还检测了麻醉废气的最大耐受剂量(不会产生临床的和病理上毒性作用的最大剂量)。经口管饲超大剂量药物时,发现氯仿和三氯乙烯对啮齿动物有致癌性,但这一给药途径与手术病人和工作人员的空气暴露不同。异氟烷、氟烷、安氟烷、甲氧氟烷和笑气吸入给药时,大量的研究结果显示其致癌性均为阴性。七氟烷和地氟烷虽然没有在小型啮齿动物进行致癌性实验,但二者都经美国FDA批准,可在临床上使用。
以长期的致癌性研究来评估吸入麻醉药的器官毒性。即使在最大耐受剂量,异氟烷、氟烷、安氟烷和笑气都没有显示对肾、肝、生殖腺和其他器官有显著的病理损害。这些麻醉药物在长期的动物研究中,均未显示出毒性,故推测,七氟烷和地氟烷也是如此。
已发表了许多吸入麻醉药对动物繁殖力影响的研究。包括:生殖能力、交配行为、胚胎、胎儿致畸、先天异常和产后存活及行为。总体而言,笑气是唯一对实验动物有直接致畸作用的吸入麻醉药物。在器官形成期,24小时给予怀孕大鼠高浓度(50%-75%)笑气和在怀孕全程给予低浓度(0.1%)笑气都会使胎儿内脏、骨骼肌异常的发生率增高。但相同的暴露条件不太可能在人类中复制。氟烷、安氟醚和异氟醚在大鼠中不会致畸。目前的共识是,这些药物的致畸作用都与给药途径、剂量相关,职业性暴露于微量麻醉废气和繁衍能力之间无相关性。七氟烷和地氟烷在由制造商赞助的研究中显示无致畸性和生殖毒性。
三、人类流行病学研究结果
自1967年Vaisman的报道后,开展了大量的对手术室工作人员健康的调查。这些调查的重点在麻醉废气对生殖能力和致癌变的有害影响上,少数也调查了对肝、肾和其他健康方面的危害。
1974年由美国麻醉医师学会(ASA)支持的关于微量麻醉气体对手术室工作人员健康影响的研究,由于受试者数量非常大,成为最引人瞩目、也是最具影响力的研究。来自不同职业机构的73,000位人员,包括ASA和美国儿科学院成员,接受了大约40,000个调查反应。同未暴露的妇女相比,暴露于麻醉废气的妇女的自行流产、肿瘤、肝脏疾病和肾脏疾病的风险升高,其后代的先天异常风险增高。暴露于麻醉废气的男性医师肝脏疾病风险增高,其子女先天异常的风险也增高。
其后十年中,完成了一些更严谨的研究。与早期的研究相比,结果并不一致,ASA委派了一个由流行病学家和生物统计学家组成的小组,对这些流行病学研究结果的统计学显著性进行了评估。该小组的文章刊载在1985年的《Anesthesiology》杂志上。Buring和同事对17篇发表的报道进行了荟萃分析。在排除了对那些包含牙医和牙医助手的、没有观察终点或没有采用对照组比较的研究后,共有6个研究纳入了荟萃分析中。结果显示,工作在手术室中妇女的自行流产风险增加30%,暴露于麻醉废气的医师其子女先天异常的风险也增加。另外,男性和女性肝脏疾病的风险增加了大约50%,女性的肾脏疾病风险增加了30%。最后还发现,宫颈癌的风险增加,而其他类型的肿瘤没有差异。
然而,调查者发现被荟萃分析的研究都存在缺陷,包括回应率低、对于无回应者、暴露麻醉药物浓度水平、混杂变量的信息、结果事件缺乏足够的信息。另外,回应者的偏向总是存在,回应者多是出现问题的,而未出现问题者可能不愿意回应调查。这些问题在Axelsson和Rylander的研究中很清晰地显示出来。他们观察到,健康风险增加很小,且可能在偏倚和未对照的混杂变量所造成的范围内。即使风险存在,也不能肯定就是微量的麻醉废气而不是其他原因造成的(诸如:放射、手术室环境中工作的应激压力等)。最近一份来自瑞典的研究显示,应激似乎很有可能成为关键原因。
调查者们相信,现有的数据不足以设置暴露的限值。他们还相信,更多的回顾性研究不太可能带来显著的有用信息,而需要更多前瞻性的研究来确定危害是否存在,是否与麻醉废气有关。即使在没有麻醉气体暴露的情况下,世界育龄妇女的自行流产率平均是达10%,新生儿有缺陷的发生率是3%。
1985年,Buring发表报道的同一年,Tannenbaum和Goldberg发表了独立的对流行病学文献进行的综述,这些文献都是关于暴露于微量麻醉废气后对生殖能力的影响。他们的结论实质上是相同的,也是建议开展更多详细的前瞻性研究并经常监测暴露水平和结局事件。他们强调,从结局事件得出的数据要仔细验证。几个另外的综述,包括Ebi和Rice的,也得出了相同的结论。
四、关于流行病学研究结果的认识
目前在我国已经废弃了动物试验研究证明有害的吸入麻醉药物,其中三氯乙烯和甲氧氟烷已经不在讨论范围内。国内仍然使用试验证明有致畸性的笑气。但致畸性是在高浓度、长时间接触后显示出来,这与实际工作环境中微量的气体浓度泄漏有很大不同,故结论的适用性有限。国内目前常用的吸入麻醉剂安氟烷、异氟烷、七氟烷,在动物实验中显示是安全的。
来自所有流行病学调查综述的结论,并不能证明暴露于手术室内的微量麻醉气体会影响健康。许多调查显示一些风险有轻到中度的增高,最引人注意的是自行流产增多,但数据收集中的偏倚和无对照的混杂变量可能是其原因,至少其可能性与手术室环境一样大。即使这些风险的增高被确认是真实的,但手术室内除了微量麻醉气体之外的其他因素也极其可能成为原因。只有专门设计的用来确认暴露于微量麻醉废气对健康影响的前瞻性研究,才有可能给出确定的答案。
迄今为止,Spench和同事分析了目前仅有的前瞻性研究。他们调查了11,500位英国的≤40岁,在医院工作的医学毕业生。收集了有关职业、工作、生活方式、内科和产科病史以及个人资料的数据。中期结果显示,女性麻醉医师不育的发生率并不高于其他医师。另外,在那些受调查者中的自行流产率和其后代先天异常发生率,与他们母亲的职业、暴露于手术室环境中的小时数或是否使用废气清除系统无关。而且,肿瘤和神经病变的发生率与职业无关。没有数据提示,微量麻醉废气对那些工作在有清除系统环境中考虑怀孕和已怀孕的女性是威胁。废气清除系统应该用于所有使用吸入麻醉药物的地方。
虽然在无麻醉气体清除系统的手术室工作导致健康损害的证据不可信,但只要在麻醉废气暴露场所使用麻醉废气清除系统并合理操作,这些场合的麻醉气泄漏浓度可被认为是在管理部门推荐的范围内。而在PACU工作的人员微量麻醉废气暴露水平低于手术室内。
1999年美国职业安全局(OSHA)关于麻醉废气的推荐意见
按照OSHA的指导说明CPL2-2.20B上提供的对个人和区域的取样办法,任何工作人员暴露于卤化物麻醉药物的废气浓度不得超过2ppm,持续时间不超过1h;当同笑气联合使用时,不得超过0.5ppm。当笑气作为单独使用的麻醉药物时,工作人员在麻醉给药时暴露水平不超过时间加权均值25ppm(荷兰也遵循此标准)。
英国推荐的职业暴露标准(OES)是8小时的加权平均值:
笑气:100ppm(意大利、瑞典、挪威、丹麦也遵循此标准)
安氟烷和异氟烷:50ppm
氟烷:10ppm
设计良好的废气清除系统由废气溢出口收集装置、手术室通风系统和限制呼吸回路正压和负压变化的方法组成。麻醉设备应由有资质的人员每季度进行维护以保证漏气最少。机构应为职员提供培训,帮助他们确立能降低不必要的麻醉废气暴露风险的操作常规。操作常规应该能使气体泄漏减少,包括在回路连接到病人之前不要开启笑气或挥发罐,不用时关闭笑气或挥发罐,以及在废气清除以前保持氧气的流量。
评估空气中麻醉废气浓度的取样步骤应该在每个麻醉地点每季度针对笑气和卤化复合物开展。监测应该包括设备的漏气测试、职员个人呼吸区域的空气取样,以及采用气囊取样或实时取样的方法监测室内空气。物理空间使用的通风和空调系统应该在规定的间期内检查和测试以保证室内空气以至少每小时15次的速度完全更换。(根据美国建筑研究院的指南,新建的医疗机构需要有能够每小时换气15到21次的系统,而且其中3次必须是室外的新鲜空气)中央真空系统要每季度检查和测试一次。
应该对那些要接受麻醉废气职业性暴露的雇员进行预先的体检。依照1988年OSHA诠释的雇员“知晓权”的要求,雇员应该被告知暴露于麻醉废气中的有害影响,包括自行流产、小儿的先天异常和对肝肾的不良影响。每个机构都要有为每个职员报告工作相关健康问题的机制。
OSHA现在还没有规定笑气和卤化药物的暴露限值。NIOSH准则文件中推荐的水平是研究中发现并能够实现的,但并没有发布。过去,OSHA对麻醉部门进行检查,如果针对工作人员的有关雇员“知晓权”条款的教育没有执行,这些部门将会被列举出来。
在1996年,英国政府健康服务咨询委员会出版了建议书,即麻醉药物:在对健康有害物质的控制管理条例下对暴露的控制(COSHH)1994版,在其中制定了职业暴露标准(OES)。OES是以8小时作为时间加权平均值的微量麻醉气浓度,如下所示。
100ppm:氧化亚氮50ppm:安氟醚和异氟醚10ppm:氟烷
因为这些浓度都低于在动物实验内出现副作用的浓度,并且没有证据表明这些浓度水平将对人体健康有影响。
一般麻醉气体在手术室内会通过两种主要途径泄漏。一个是涉及到麻醉给药的技术,而另一个涉及麻醉药传输系统和清除系统的硬件设备。任何一个环节出问题都将导致手术室内空气的严重泄漏污染。(表2)
表2 手术室泄漏污染的原因及推荐做法

(一)麻醉技术的问题
吸入性麻醉药发生泄漏常涉及到技术问题。最常见的情况是当病人断开麻醉回路时没有关闭所有流量控制阀(包括氧气,氧化亚氮和空气)或者挥发罐。另外,不匹配的面罩,特别是当病人存在困难气道时,特别容易使麻醉气体泄漏于室内。同样,许多医师为了让病人快速从麻醉中苏醒过来而在手术结束时以大量氧气冲洗回路。如果被冲洗出的气体是进入手术室内而不是进入清除系统,也将导致室内污染。最后,当采用吸入麻醉的病人脱开回路自主呼吸时,麻醉气体也将泄漏于手术室内。
麻醉挥发罐的填充也会导致手术室内污染。1毫升的液体的吸入麻醉药物在室温下将挥发成近200ml的气体。麻醉挥发罐配有两套填充系统。“加药器引导”的系统更少发生麻醉药物的溢出,而漏斗填充式易发生麻醉液体泄漏。地氟烷挥发罐的专利填充系统可确保在填充时没有液体溢出。
麻醉机和清除系统
目前销售的麻醉机都配有清除麻醉废气的清除系统。清除系统收集经可调节压力限制阀(APL)或“瞬间排出”阀或呼吸机压力释放阀等处呼出释放的气体,并将它们送到废气处理系统(图1)。与清除系统相匹配的接头标准直径是19mm,但新的国际标准是30mm。新型的麻醉机有30mm接口,厂家能提供将19mm转换成30mm的适配器(图1)。通常麻醉回路中泄漏的气体都通过废气清除系统清除。仅当在麻醉气体输送或清除系统中有泄漏、或输送至清除系统的气体超过能被排除的气体量时,麻醉气体将泄漏入房间。使用麻醉机前必须检查废气清除系统功能是否正常。
废气清除系统按紧闭的或开放的存储器分成两种。在紧闭存储系统中,气体将从麻醉回路中的APL阀或呼吸机压力释放阀进入清除系统。两者的接合处安装了一个正压释放(“瞬间排除”)阀用来将系统内过多的气体排入室内而防止压力过度升高,还安装了一个或多个负压释放阀,通过允许室内空气进入系统来防止接合处负压过大。紧闭的存储系统安装有一个存储囊来补偿气体进出清除界面时的急速变化。通过清除系统的连接处,废气进入废气处理系统(图片2a, 2b)。
清除系统的开放存储器系统是无阀门设计,使用一个通向大气的存储罐使正压或负压自由释放。另外,从麻醉回路APL和呼吸机PR阀引出的废气通向开放存储器系统,医院的废气处理系统也与存储器相接。(图3)。
清除系统的连接处容易发生几个潜在问题。如果输送来自麻醉回路的APL或呼吸机PR阀的软管打折或阻塞,病人可能发生呼吸道气压伤。如果连接医院气体处理系统的管路受阻,而麻醉气体将会通过压力释放阀进入大气。但如果这个释放阀门无法正常工作,病人也将产生气压伤。而且,通常连接处的接口数量比用的要多,所以对这些多余接口要装上密闭的盖子,以防止麻醉气体泄漏入房间(图2b)。
当废气通过连接处后,将传送入医院的气体处理系统。这时的清除可由主动的或被动的机制来完成。在主动系统,废气将由真空管主动清除。在连接处有流量控制阀,可以让操作者在任何时间调节真空压力的大小。如果真空管没有被正确调节或与连接处脱开,麻醉气体将会溢入房间。在连接处的存储囊同时可作为可视指示器,来判断此系统的真空压的大小是否合适。主动系统的真空管由医院的负压吸引系统来建立。对于废气的清除系统最好有独立于的真空系统。
在被动型的气体排除系统中,软管从清除系统的连接处通到手术室的通风排出系统。废气排出到室外。如果使用这种系统,则手术室的通风系统必须是不循环的。麻醉气体趋向于从排气栅格流出,因为手术室的通风系统使室内维持轻度的负压。这种系统的危险是软管被压迫或阻塞时,气体将释放入室内。因此软管不应该放置在地板上,而且应该用不易压缩的材料制成。在被动系统中,如果医院的气体出口处被碎废片或冰块所堵塞,那样清除的气体将不能被排到室外。高风速也会导致气体在此系统中倒流。
无论气体清除系统是主动还是被动,它应该始终通过连接处进行连接。这将大大减少病人气压伤的发生,也为所有管道提供了方便的连接点。
手术室内污染的主要原因是麻醉气体输送和清除系统中的气体泄漏。高压氧化亚氮软管和麻醉机上的氧化亚氮瓶同样可以导致大量气体泄漏,因为这些系统中的压力常超过50磅/平方英寸(psig)。如果氧化亚氮瓶不能和麻醉机的接头匹配,则将有大量的氧化亚氮泄漏入空气,因为在瓶内的压力超过700psig。麻醉机或回路系统的任何一部分接合不匹配或有漏洞都将导致麻醉气体进入室内。这常发生在那些变形或被坚硬物刺破的塑料软管,或O型环破裂。同时,如果挥发罐的填充盖子没有盖好,也是大量泄漏的原因之一。最后,在两部分用橡胶接口连接处,如橡胶破裂、磨损或接口部分没对准,泄漏也将发生。这种的典型例子是二氧化碳吸收罐。在麻醉机的低压系统的泄漏(流量控制阀的所有下游区域)常能被仔细的泄漏检测所发现。高压系统部分的泄漏可被泄漏监测或手术室内空气监测所发现。
另外两种不受麻醉医师直接控制的手术室内污染是冷冻手术和体外循环机。许多冷冻手术室用的氧化亚氮在高于90L/min的水平。如果不被清除,手术室内严重的污染将发生。另外,强效的吸入挥发性麻醉药物常用于体外循环中。因此,从体外循环回路出来的气体必须清除。因此必须有独立的清除系统。
一旦任何麻醉气体溢入手术室内,气体清除就靠手术室内通风系统。新型的手术室需要有能与外界进行每小时15-21次的气体交换,其中3次是室外的新鲜气体。重要的是维护部门要定期检查每个手术室的换气是否足够。非循环型的通风系统通过每次气体交换给手术室内带来新鲜的空气。这种系统比循环型的通风系统能更快地降低了手术室空气中的麻醉药物浓度。循环系统部分交换手术室内的空气,加入新鲜空气混合。在每个小时内,也有特定数量的新鲜气体交换。循环系统在加热和空调中有明显的节能优势。
监测手术室内空气中的麻醉气体浓度可有助于发现泄漏。一些机构发现高压泄漏常发生在麻醉机的使用中。下面的方法能对手术室环境空气中的麻醉废气微量浓度进行取样。
此方法能监测由高压系统(例如,氧化亚氮管道,机器的高压系统)泄漏造成的稳定浓度水平(未使用时)的气体水平。简单取样只能在非工作的时候,例如在没有麻醉术进行时,从手术室内提取空气样本。空气将被取样放入惰性气体的存储器内密闭,然后送入实验室分析。因为在麻醉过程中气体泄漏通常是间断的,所以对无麻醉时进行的手术室取样也许不能有效地检测使用过程中的手术室内微量气体浓度水平。另一个不足是这些结果都会有延迟。
用来评估一段时间内平均的暴露程度。这种方法中,每小时或每8小时,运用一种泵来连续收集手术室内空气样本并装入袋内,供分析使用。小型时间加权平均取样泵和囊也常使用,但这用于研究的目的,而针对现实中大量人员的监测并不可行。被动放射测定仪,类似于在放射科工作人员佩戴的照射量测定徽章,可用于有效监测氧化亚氮暴露浓度。它们被放置在手术室内工作人员的呼吸地带,从1小时到168小时均可使用。放射测定仪在暴露开始时打开盖子,而在暴露结束时则盖上盖子。佩戴者将有一个暴露周期的纪录,在取样结束时,徽章将标记上职员的名字和暴露时间,然后送往外部实验室。通过分析徽章里被捕捉的氧化亚氮得到结果,结果以每小时每百万分之一的浓度代表。除了监测个人暴露程度,徽章也被用于固定区域的监测。
是一种可连续取样和分析挥发性麻醉药物浓度的便携式红外分析仪,用于监测手术室内空气的最简便的方法。该仪器可连续读出空气中麻醉气体浓度,也被用来“嗅闻”设备的气体泄漏。如果在长时间内连续取样,会显示时间加权平均浓度。它能用于发现周围空气中麻醉气体浓度(N2O:0-100ppm, 挥发性麻醉气体:0-10ppm)。
八、七氟烷与复合物A
七氟烷已经成为国内吸入麻醉的主流药物。七氟烷与呼吸回路中吸收CO2的钠石灰(成分:氢氧化钙、氢氧化钠、氢氧化钾)接触,会产生复合物A(compound A,fluoromethyl-2,2-difluoro-1-(trifluoromethyl)vinyl ether),尤其是在高温和干燥的环境下产生得更多,因此在低流量吸入麻醉时明显增加。复合物A在大鼠试验中可导致肾坏死(浓度:25-50 ppm)和死亡(浓度:130-340 ppm),但在人类并没有发现肾毒性的病理学证据(一般在临床吸入麻醉中,复合物A可以很容易达到25-50 ppm),仅发现有剂量相关性的蛋白尿、糖尿和酶尿,从未有过严重肾脏功能损害病例的临床报告。
目前不建议在新鲜气流量低于1L/min下,使七氟烷的用量达到2MAC•小时,低流量时应注意每小时定期增大流量行半关闭回路2~3min。世界上只有加拿大和澳大利亚规定新鲜气流量不得低于2L/min,大于这个流量可以无限制地使用。
为了减少复合物A的产生,除了避免低流量外,还可以使用含有氯化钙和硫酸钙的新型CO2吸收剂,它不与七氟烷起反应,可使呼吸回路中的复合物A始终保持在3.3 ppm以下。复合物A泄露于大气中对周围工作人员的健康影响尚无研究,但由于极其微量,因而推测应无任何影响。
推荐意见:麻醉废气清除系统应该广泛应用于所有麻醉废气暴露场所。每个机构都有责任制定麻醉设备的维护和检查程序,包括废气清除系统,并以文档形式证明。
推荐理由:虽然没有证据证实微量的麻醉废气会危害人体健康,但是通过废气清除系统来减少废气暴露这一保护措施已广泛受到认可。
推荐意见:使所有相关人员采用有效措施来减少周围空气中麻醉废气的浓度水平。
推荐理由:关注操作常规的细节对于减少麻醉废气的暴露是有效的。
推荐意见:不推荐在废气暴露场所一定要安装监测设备,没有数据证明这是必要的。
推荐理由:使用麻醉废气清除系统可以有效地减少手术室内麻醉废气的浓度,使其浓度维持在NIOSH的推荐阈值浓度下。当必要时,例如(麻醉设备仪器损坏),可按照上述办法测量麻醉废气浓度。
推荐意见:不强制规定对暴露于麻醉废气的医护人员进行常规健康检查,但是需要对相关的医护人员进行麻醉废气相关知识教育:包括以往文献结论的分析,如何改善操作常规来减少麻醉废气以及麻醉废气清除系统的检查、维护等。并且要建立一个麻醉废气危害的报告机制,一旦发现麻醉废气对人体健康产生危害,就能上报。
推荐理由:最新的数据不能表明微量的麻醉废气会对相关的医护人员的健康产生危害,尤其是在有麻醉废气清除系统的环境中。
研究表明,在有废气清除系统的麻醉工作场所中,微量麻醉气体对工作人员的健康没有任何不利影响。
手术室应配备麻醉废气清除系统;
建立规范的手术室操作常规,使麻醉废气室内泄漏最小化;
对于相关工作人员进行教育,包括:麻醉废气对工作人员的影响,通过规范的操作常规来减少废气,麻醉废气清除系统设备维护等;
目前尚不推荐对手术室或PACU的麻醉气体浓度水平进行常规监测;
目前尚不推荐对暴露于微量麻醉气体中的工作人员的健康进行常规检查,但是每个存在麻醉废气泄漏的机构都应有相关的应对措施和制度,工作人员可随时报告可疑的、与工作相关的健康隐患问题。
麻醉气体泄漏对相关工作人员健康的影响还有争议,需要前瞻性、双盲对照、多中心的临床研究结果证实。
麻醉气体泄漏的清除系统应作为常规要求进行建设。
没有证据证明,在有麻醉废气清除系统的地方,微量浓度的麻醉气体会对医护人员的健康有不利的影响。在这些地方怀孕和工作是安全的。
无须因此对相关人员进行常规体检,但主张积累、统计这些人员的相关健康问题。
图1 呼吸环路与密闭废气贮气袋接口
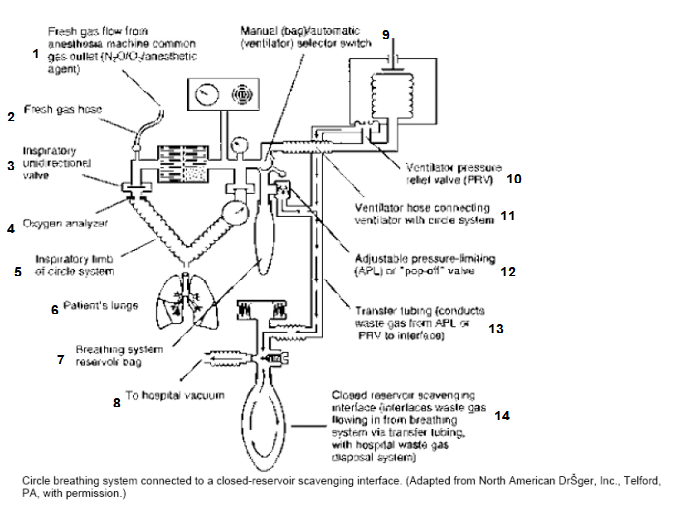
1.来自麻醉机公共出口的新鲜气体(笑气/氧气/麻醉药物)
2.新鲜气体软管
3.吸气单向阀
4.氧气分析仪
5.呼吸回路系统的吸气端
6.病人肺
7.呼吸系统贮气袋
8.到医院真空吸引
9.手动(贮气袋)/自动(通气机)选择开关
10.呼吸机压力释放阀(PRV)
11.连接回路系统与呼吸机的软管
12.可调式压力限制(APL)阀或“瞬间排出”阀
13.传输管道(将废气从APL或PRV输送到接口)
14.紧闭的废气存贮器清除接口(来自呼吸系统的废气经传输管道进入的医院的废气清除系统)
图2a北美Drager麻醉机的密闭贮气清除接口。A位置表明贮气袋膨胀度正常。B位置是过度膨胀。C位置是因真空压过大,气袋塌陷。
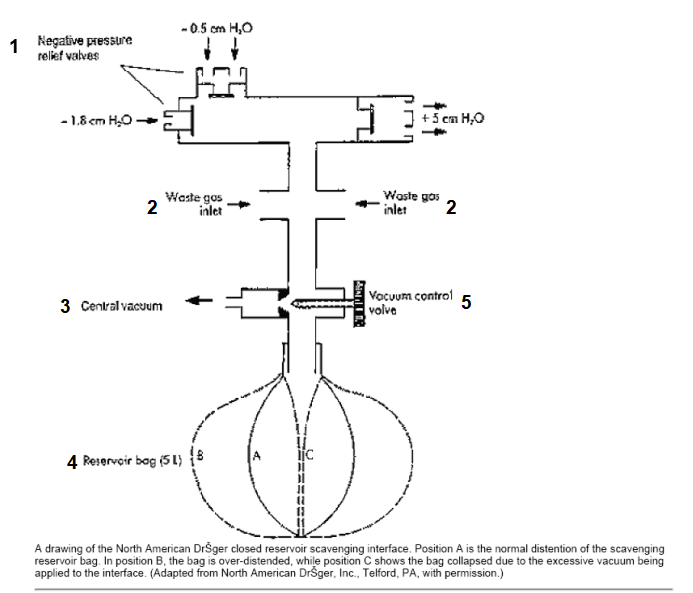
1.负压释放阀
2.废气入口
3.中央真空吸引
4.贮气袋(5L)
5.真空控制阀
图2bDatex-Ohmeda 麻醉机的密闭废气贮气袋与主动清除接口
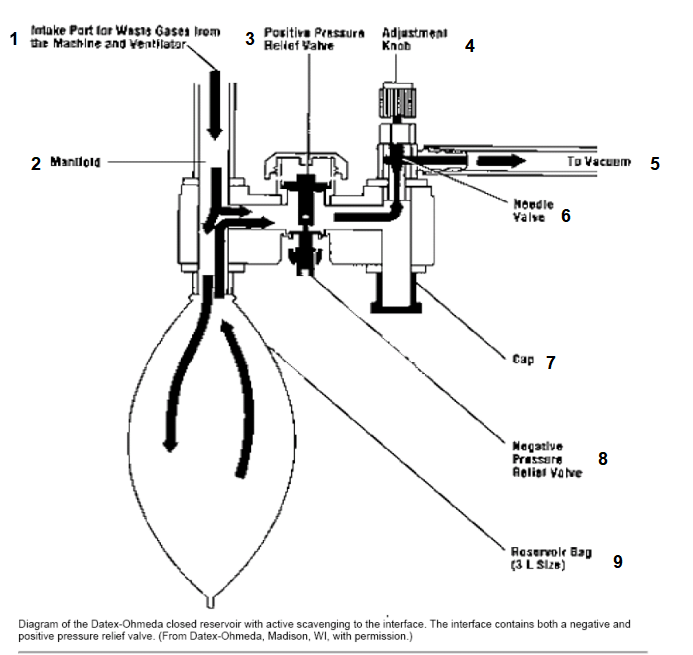
1.麻醉机和呼吸机废气进入部分
2.复合管道
3.正压释放阀
4.调节钮
5.到真空吸引
6.针孔阀
7.帽子
8.负压释放阀
9.贮气袋(5L)
图3 北美Drager公司的开放贮气清除系统
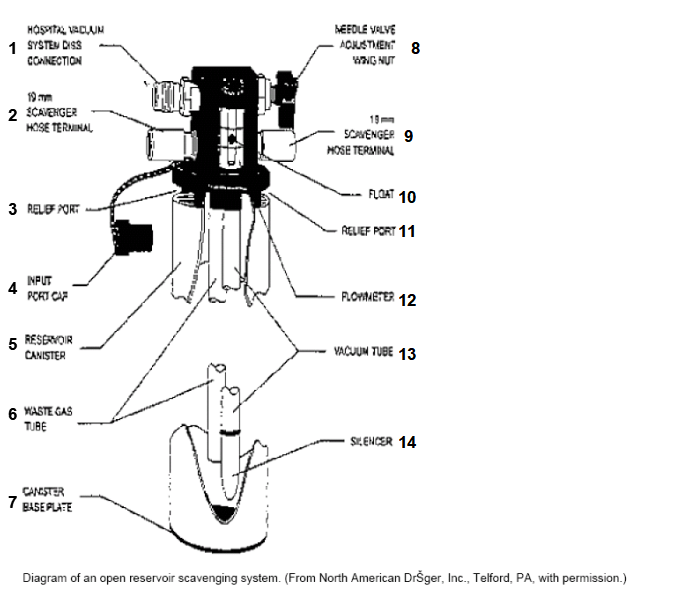
1.医院真空系统DISS接头
2.19mm清除器软管终端
3.释放端口
4.入口帽
5.存贮罐
6.废气管
7.罐子的底座
8.调节针孔阀的蝶形螺母
9.19mm清除器软管终端
10.浮子
11.释放端口
12.流量计
13.真空管
14.消音器
参考文献
1Eger EI II, White AE, Brown CL, Biava CG, Corbett TH, Stevens WC. A test of the carcinogenicity of enflurane, isoflurane, halothane, methoxyflurane, and nitrous oxide in mice. Anesth Analg. 1978; 57:678-694.
2 Baden JM, Kundomal YR, Mazze RI, KosekJC.Carcinogen bioassay of isoflurane in mice. Anesthesiology. 1988; 69:750-753.
3 Baden JM, Kundomal YR, Luttropp ME Jr, Mazze RI, KosekJC.Carcinogen bioassay of nitrous oxide in mice.Anesthesiology. 1986; 64:747-750.
4 Baden JM, Egbert B, MazzeRI.Carcinogen bioassay of enflurane in mice.Anesthesiology.1982; 56:9-13.
5 Baden JM, Mazze RI, Wharton RS, Rice SA, Kosek JC. Carcinogenicity of halothane in Swiss/ICR mice.Anesthesiology. 1979;
6Chloroform as an ingredient of human drug and cosmetic products. Federal Register. 14:15026. DHEW, FDA, 1976.
7 Carcinogenesis technical report series. No. 2: Carcinogenisis bioassay of trichloroethlene. CAS No. 79-01-6. National Cancer Institute, 1976.
8 Shepard TH. Fink BR. ed. Teratogenic Activity of Nitrous Oxide in Rats. In: Toxicity of Anesthetics. Baltimore, MD: Williams and Wilkins; 1968:308-323.
9 Vieira E, Cleaton-Jones P, Austin JC, Moyes DG, Shaw R. Effects of low concentrations of nitrous oxide on rat fetuses. Anesth Analg.1980; 59:175-177.
10 American Society of Anesthesiologists Ad Hoc Committee on the Effect of Trace Anesthetics on the Health of Operating Room Personnel. Occupational disease among operating room personnel: A national study. Anesthesiology.1974; 41:321-340.
11 Knill-Jones RP, Rodrigues LV, Moir DD, Spence AA.Anaesthetic practice and pregnancy. Controlled survey of women anaesthetists in the United Kingdom. Lancet.1972; 1:1326-1328.
12 Rosenberg P, Kirves A. Miscarriages among operating theatre staff.ActaAnaesth Scand. 1973; 53:37-42.
13 Axelsson G, Rylander R. Exposure to anaesthetic gases and spontaneous abortion: Response bias in a postal questionnaire. Int J Epidemiol.1982; 11:250-256.
14 Spence AA, Knill-Jones RP. Is there a health hazard in anaesthetic practice? Br J Anaesth.1978; 50:713-719.
15 Cohen EN, Bellville JW, Brown BW Jr. Anesthesia, pregnancy, and miscarriage: A study of operating room nurses and anesthetists. Anesthesiology.1971; 34:343-347.
16 Axelsson G, Ahlborg G, Jr., Bodin L. Shift work, nitrous oxide exposure, and spontaneous abortion among Swedish midwives. Occup Environ Med. 1996; 53:374-378.
17Spence AA. Environmental pollution by inhalation anaesthetics.Br J Anaesth.1987; 59:96-103.
18 Friedman JM. Teratogen update: Anesthetic agents. Teratology.1988; 37:69-77.
19 American Institute of Architects: Guidelines for Construction and Equipment of Hospitals and Medical Facilities. Washington, DC,1992.
20Murray JM, Renfrew CW, Bedi A, et al: A New Carbon Dioxide Absorbent for Use in Anesthetic Breathing Systems. Anesthesiology, 91(5) : 1342-8,1999
首页封面图片来源网络,侵删
